Балаболкин атопический дерматит у детей
Комментарии
ЖУРНАЛ «ПРАКТИКА ПЕДИАТРА»
Опубликовано в журнале:
«Практика педиатра», декабрь 2010, с. 58-60
В.А. Булгакова, доктор медицинских наук, главный научный сотрудник, Научный центр здоровья детей РАМН, Москва
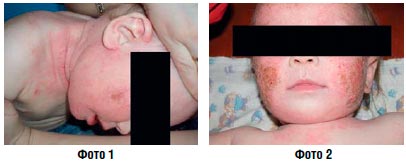
Атопический дерматит (АтД) – одно из наиболее распространенных в мире кожных заболеваний у детей, причем в последние годы отмечается тенденция к его тяжелому клиническому течению [1–3]. АтД является первым проявлением «атопического марша» и значимым фактором риска развития бронхиальной астмы у детей, так как его патоморфоз характеризуется не только локальным воспалением кожи, но и системным иммунным ответом с вовлечением в процесс респираторного тракта [3].
Среди факторов развития АтД рассматривают наследственную отягощенность по аллергическим заболеваниям, сухость кожных покровов, снижение порога зуда и нарушения со стороны иммунной системы [1, 4, 5]. Активация иммунной системы, а именно Т-лимфоцитов, индукция апоптоза кератиноцитов, синтез IgE, вовлечение эозинофилов являются основой аллергического воспаления при АтД. Запуск каскада иммунологических реакций происходит после проникновения аллергенов через нарушенные барьеры кожных покровов и слизистой оболочки пищеварительного тракта. Аллергены попадают в глубокие слои кожи за счет выраженной сухости кожных покровов, нарушения потоотделения, снижения уровня церамидов и трансэпидермальной потери воды. Проникновение аллергенов через желудочно-кишечный тракт возможно вследствие повышенной проницаемости слизистой оболочки кишечника, незрелости ее барьерной функции и недостаточной продукции секреторного IgA [6].
Атопический дерматит (в МКБ-10, раздел L20) – хроническое воспалительное заболевание кожи, сопровождающееся зудом, возрастной морфологией высыпаний, стадийностью, частым инфицированием. У детей раннего возраста ведущими в развитии АтД являются пищевые аллергены. После 3 летнего возраста значение пищевой сенсибилизации уменьшается и возрастает роль ингаляционных аллергенов. Неспецифическими триггерными факторами, провоцирующими обострение атопического дерматита, являются ирританты (одежда из шерсти и синтетических тканей, детергенты, табачный дым), эмоции, стрессы, климатические факторы (холодное время года, резкая смена климата), поллютанты. Одним из триггерных факторов, запускающих каскад иммунных реакций при АтД, являются микроорганизмы, колонизирующие кожные покровы. Рецидивирующему, упорному течению АтД способствует колонизация поверхности кожи Staphilococcus aureus и грибами рода Malassezia furfur (Pityrosporum ovale), не только поддерживающая воспаление, но и приводящая к сенсибилизации организма. Считается, что ряд токсинов St. aureus, обладающих свойствами суперантигенов, играют ведущую роль в развитии и поддержании воспаления кожи при АтД [5]. При этом не только присоединение пиодермии, но и бессимптомное носительство St. aureus у пациентов с атопическим дерматитом усугубляют тяжесть и длительность обострений дерматита. Так, например, 90% больных АтД – носители St. aureus, а у 60% обнаруживают ассоциации стафилококка и стрептококка. При локализации высыпаний на коже лица и шеи в 100% выявляют лабораторные признаки инфицирования грибами Pityrosporum ovale [7].
Терапия АтД направлена на устранение специфических и неспецифических триггерных факторов, разрешение аллергического воспаления кожных покровов, нормализацию работы желудочно-кишечного тракта, борьбу с сухостью кожных покровов и восстановление поврежденного липидного слоя [4, 5, 8]. Лечение осложненных пиодермией и грибковой инфекцией форм АтД предусматривает проведение адекватной наружной и этиотропной терапии, коррекцию иммунологических нарушений с использованием иммуномодулирующих средств [6–9]. На сегодняшний день считается клинически оправданным и эффективным применение иммунотропных препаратов при осложненных вторичной инфекцией формах АтД, одним из которых является отечественный синтетический высокомолекулярный иммуномодулятор Полиоксидоний® (МНН: азоксимера бромид), что подтверждает многолетний опыт его применения (разрешен к применению в практике с 1996 г.).
Иммунотропный эффект Полиоксидония® заключается в нормализующем влиянии на продукцию провоспалительных цитокинов, в усилении цитотоксической активности NK-клеток, в повышении естественной резистентности организма к бактериальным и вирусным инфекциям [10], что было подтверждено и исследованиями в нашей клинике. Включение в комплексную терапию Полиоксидония® больным с тяжелым течением бронхиальной астмы и вторичной иммунной недостаточностью позволило увеличить время ремиссии хронических очагов инфекции и основного заболевания, сократить длительность пребывания в стационаре, улучшить показатели иммунного ответа [11]. При назначении Полиоксидония® пациентам с дермореспираторным синдромом отмечалось снижение частоты острых респираторных вирусных инфекций и обострений как респираторной, так и кожной аллергии [12].
Влияние Полиоксидония® на иммунитет является иммуномодулирующим, то есть зависящим от исходной функциональной активности иммунной системы. Полиоксидоний® оказывает сложное и многогранное воздействие на иммунную систему. Так как развитие любого иммунного ответа начинается с клеток моноцитарно-макрофагальной системы, а цитокины, продуцируемые моноцитами/макрофагами, обладают плейотропным эффектом, усиление их функциональной активности под влиянием полиоксидония ведет к активации клеточного и гуморального иммунитета [10].
Полиоксидоний® обладает широким спектром фармакологического воздействия на организм, который помимо иммуномодулирующего включает антиоксидантное, детоксицирующее, мембранопротекторное и хелатирующее. Иммунотропная терапия Полиоксидонием® проводится в период обострения АтД, осложненного вторичной инфекцией, на фоне комплексного лечения с парентеральным введением антибиотиков, антигистаминных препаратов, системных ГКС, инфузионной терапии [13].
Безопасность и эффективность применения Полиоксидония® подтверждена исследованиями, проведенными как у взрослых, так и у детей: пациенты, страдающие АтД, хорошо его переносят, ни в одном случае не отмечены реакции и изменения в клинических и биохимических показателях крови и мочи при приеме препарата [10]. Применение Полиоксидония® в комплексной терапии АтД увеличивает длительность ремиссии, в 2 раза сокращает проявления дерматита, в 2,5 раза снижает дозировку применяемых совместно глюкокортикостероидов (ГКС) [13, 14]. При АтД, осложненном бактериальной, вирусной, грибковой инфекцией, применение Полиоксидония® в сочетании с антибиотиками способствует более быстрому (в 2,5 раза) уменьшению воспалительной инфильтрации кожи и в 1,6 раза позволяет сократить продолжительность антибиотикотерапии [14, 15].
Полиоксидоний® можно использовать как с целью коррекции местного иммунитета, так и для системной терапии. Препарат выпускается в виде лиофилизированного порошка для инъекций и местного применения в ампулах, флаконах, содержащих 3 и 6 мг азоксимера бромида (применяется у детей с 6 месяцев), суппозиториев ректальных по 6 и 12 мг (применяется у детей с 6 лет) и таблеток (12 мг) назначаемых сублингвально детям с 12 лет [16]. При комплексном лечении осложненных вторичной инфекцией форм АтД у детей может применяться следующая схема лечения: доза Полиоксидония® выбирается из расчета 70–150 мг/кг, в зависимости от тяжести процесса, препарат вводят в/м или в/в, через 1–2 дня общим курсом 5–7 инъекций или в форме суппозитория (6 мг) первые 3 дня, а затем – с интервалом 48 часов, курс № 10–15.
Использование Полиоксидония® в комплексной терапии, направленной на купирование обострения АтД, осложненного вторичной инфекцией, значительно уменьшает признаки общей интоксикации, способствует более быстрому купированию воспалительного кожного процесса, что коррелирует с нормализацией показателей иммунного статуса в виде усиления фагоцитирующей способности нейтрофилов и моноцитов.
Список литературы:
- Балаболкин И.И., Гребенюк В.Н. Атопический дерматит у детей. М.: Медицина, 1999. 240 с.
- Короткий Н.Г., Тихомиров А.А., Таганов А.В., Моисеенко А.В. Атопический дерматит у детей. Тверь: Триада, 2003. 238 с.
- Детская аллергология / под редакцией А.А. Баранова, И.И. Балаболкина. М.: ГэотарМедиа, 2006. 687 с.
- Аллергология иммунология. Клинические рекомендации для педиатров / под общей редакцией А.А. Баранова и Р.М. Хаитова. М.: Союз педиатров России, 2008. 248 с.
- Атопический дерматит и инфекции кожи у детей: диагностика, лечение и профилактика. Научно-практическая программа. – М., 2004, 58 с.
- Смирнова Г.И. Современные подходы к лечению и реабилитации атопического дерматита, осложненного вторичной инфекцией // Аллергология и иммунология в педиатрии. 2004. № 1. С. 34–39.
- Лечение аллергических болезней у детей / под редакцией И.И. Балаболкина. М.: ООО «Медицинское информационное агентство», 2008. 352 с.
- Maчapaдзe Д.Ш. Атопический дерматит у детей. М.: Триада, 2005. 288 с.
- Лусс Л.В. Принципы применения иммуномодулирующей терапии у больных с атопическими заболеваниями, протекающими в сочетании с синдромом вторичной иммунной недостаточности // Аллергология и иммунология. 2002. Т. 3, № 1. С. 159–163.
- Полиоксидоний в клинической практике / под ред. А.В. Караулова. М.: ГЭОТАР-Медиа, 2008. 136 с.
- Кузнецова Н.И., Балаболкин И.И., Кузнецов О.Ю. Применение полиоксидония при бронхиальной астме у детей // Иммунология. 2003. № 5. С. 293–295.
- Рылеева И.В., Булгакова В.А., Балаболкин И.И. и др. Иммуномодулирующие препараты в терапии бронхиальной астмы у детей // Вопросы современной педиатрии. (Приложение). 2006. Т. 5, № 1 С. 505.
- Казначеева Л.Ф., Галеева Е.А., Молокова А.В. и др. Применение Полиоксидония в комплексной терапии атопического дерматита у детей. URL: polyoxidonium.ru/articles/ped/04.htm
- Цывкина Г.И. и др. Полиоксидоний в лечение больных с атопическим дерматитом // Применения Полиоксидония в педиатрии (в помощь практическому врачу). М., 2005. 25 с.
- Феденко Е.С., Варфоломеева М.И., Латышева Т.В. Применение Полиоксидония у больных с атопическим дерматитом // Лечащий врач. 2001. № 4. С. 52–53.
- Государственный реестр лекарственных средств. – М.: МЗиСР. URL: www.drugreg.ru
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Комментарии
Опубликовано в журнале:
«ПРАКТИКА ПЕДИАТРА»; февраль; 2016; стр.54-59
В.Р. Воронина, врач-дерматовенеролог, к. м. н., ГБОУ ВПО «Российский национальный исследовательский университет им. Н.И. Пирогова», Обособленное структурное подразделение — Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева
Сокращения: ТГКС — топические глюкокортикостероиды, ТИК — топические ингибиторы кальциневрина, АтД — атопический дерматит
Ключевые слова: атопический дерматит, наружная терапия, базовая терапия, топические глюкокортикостероиды, топические ингибиторы кальциневрина
Key words: atopic dermatitis, topical treatment, basic treatment, topical corticosteroids, topical calcineurin inhibitors
Атопический дерматит (АтД) — мультифакторное заболевание кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом, обусловленное гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям [1, 2]. Заболевание в типичных случаях начинается в раннем детском возрасте и значительно нарушает качество жизни больного и членов его семьи. Распространенность среди детского населения составляет до 20%, тогда как у взрослых достигает только 1-3% [2]. Лечение АтД должно быть комплексным и патогенетически обоснованным, включающим элиминационные мероприятия, диету, гипоаллергенный режим, местную и системную фармакотерапию, обучение больного и членов его семьи [3]. Наружная терапия является абсолютно необходимой для достижения улучшения состояния и должна проводиться дифференцированно с учетом изменений кожи, мультифакторного генеза заболевания (интегральный подход) [4, 5].
При назначении терапии следует включать:
Всем больным АтД вне зависимости от тяжести, распространенности, остроты кожного процесса, наличия или отсутствия осложнений назначаются средства базового ухода за кожей. Базовая терапия должна включать рациональный уход за кожей, направленный на восстановление нарушенной функции кожного барьера путем использования смягчающих и увлажняющих средств, средств для очищения кожи, а также выявление и устранение контакта со специфическими и неспецифическими триггерами [5].
Купание ребенка с АтД является необходимой процедурой, позволяющей очистить кожу от нанесенных ранее слоев препаратов, слущивающихся чешуек эпидермиса, корок. Очищение кожи позволяет достигнуть непосредственного контакта лекарственного средства с кожей. Исключением является наличие очагов выраженного мокнутия, вторичного инфицирования кожи. В этот период целесообразно воздержаться от принятия ванной, общего душа в течение нескольких дней, для того, чтобы избежать диссеминации инфекции. Далее купание можно проводить ежедневно, соблюдая комфортную для малыша температуру воды. Вода для купания должна быть 35-36 градусов и желательно дехлорированной (отстаивание воды в течение 1-2 часов). Один-два раза в неделю используются не щелочные моющие средства (так называемые синдеты), без использования жестких мочалок. Высушивание кожи проводится промокающими движениями, без травмирующего растирания кожи. После очищения кожи необходимо обработать расчесы, трещины раствором антисептика (фукорцин, зеленка, мирамистин или др.). Это позволяет свести к минимуму риск вторичного инфицирования и возникновения инфекционно-зависимых обострений дерматита, избежать попадания компонентов наружных средств на участки с нарушенной целостностью кожных покровов, ведущее к возникновению неприятных субъективных ощущений в виде жжения и зуда.
Сразу после купания необходимо использование увлажняющих, релипидирующих средств по уходу за кожей. Это позволяет удержать влагу в эпидермисе, исключить пересыхание кожи [6, 7]. Следует избегать нанесения средств косметического ухода за кожей на очаги острого и подострого воспаления. Конкретный препарат и его лекарственная форма подбираются индивидуально на основании предпочтений пациента, индивидуальных особенностей кожи, сезона, климатических условий, а также времени суток.
Общие рекомендации по применению увлажняющих и смягчающих средств согласно федеральным клиническим рекомендациям по лечению атопического дерматита [2]:
Средства с противовоспалительной активностью выбираются в соответствии со стадией воспалительного процесса (табл.) [7,11].
Таблица.
Применение лекарственных форм при различных стадиях атопического дерматита
Количество топического препарата для наружного применения измеряется согласно правила «длины кончика пальца» (FTU, FingerTipUnit), при этом одна 1 FTU соответствует столбику мази диаметром 5 мм и длиной, равной дистальной фаланге указательного пальца, что соответствует массе около 0,5 г. Этой дозы топического средства достаточно для нанесения на кожу двух ладоней взрослого человека, что составляет около 2% всей площади поверхности тела. Наружные противовоспалительные лекарственные средства необходимо наносить на увлажненную кожу, непосредственно на очаги поражения кожи. Их применение прекращают при разрешении процесса и переходят на базовую терапию. В последнее время рекомендуют метод проактивного лечения: длительное использование малых доз топических противовоспалительных препаратов на пораженные участки кожи в сочетании с применением эмолиентов на весь кожный покров и регулярное посещение дерматолога для оценки состояния кожного процесса [2,12]. Эффективность наружной терапии зависит от трех основных принципов: достаточная сила препарата, достаточная доза и правильное нанесение. При атопическом дерматите с противовоспалительной целью используются топические глюкокортикостероиды, топические ингибиторы кальциневрина, активированный пиритоин цинка. Также возможно использование экстемпоральных мазей, паст, примочек, имеющих в своем составе салициловую кислоту, вазелин, вазелиновое масло, метилурацил, ланолин, нафталан, ихтиол, дерматол, цинк, крахмал, висмут, тальк, борную кислоту, йод, масло оливковое, они обладают комплексным противовоспалительным, кератолитическим, кератопластическим, дезинфицирующим, высушивающим действием.
На сегодняшний день основой местной терапии при обострениях АтД являются топические глюкокортикостероиды (ТГКС). Выбор ТГКС определяется тяжестью течения и обострения. Согласно Европейской классификации (Miller J., Munro D., 1980), выделяют четыре класса данных препаратов в зависимости от их активности. Основные глюкокортикостероидные препараты, рекомендуемые для лечения АтД у детей: гидрокортизон, флутиказона пропионат, мометазона фуроат, гидрокортизона бутират, метилпреднизолона ацепонат. Наружные глюкокортикостероидные препараты наносят на пораженные участки кожи от 1 до 3 раз в сутки, в зависимости от выбранного препарата и тяжести воспалительного процесса. Не рекомендуется разведение официнальных топических препаратов индифферентными мазями, так как такое разведение изменяет концентрацию действующего вещества, но не снижает частоту появления побочных эффектов. Необходимо избегать использования ТГКС высокой активности на кожу лица, область гениталий и интертригинозные участки. Для этих областей обычно рекомендуются ТГКС с минимальным атрофогенным эффектом (мометазона фуроат, метилпреднизолона ацепонат, гидрокортизона-17-бутират). Во избежание резкого обострения заболевания дозу ТГКС следует снижать постепенно. Это возможно путем перехода к ТГКС средствам меньшей степени активности с сохранением ежедневного использования или путем продолжения использования сильного ТГКС, но со снижением частоты аппликаций (интермиттирующий режим) [2, 13]. В ряде клинических исследований было показано, что использование топических ТГКС совместно со смягчающими/увлажняющими средствами позволяет уменьшить курсовую дозу ТГКС [14].
При наличии или подозрении на инфекционное осложнение показано назначение ТГКС, комбинированных с антибиотиками и противогрибковыми средствами (фото 2, 5). Следует учитывать. Что многие комбинированные препараты содержат высокоактивный бетаметазона дипропионат, применение которого у детей нежелательно.
Группа топических ингибиторов кальциневрина (ТИК) включает такролимус и пимекролимус. Фармакологическое действие ТИК обусловлено ингибированием кальциневрина и дальнейшего выделения Т-лимфоцитами и тучными клетками воспалительных цитокинов и медиаторов.
Общие рекомендации по применению ТИК [13]:
Такролимус — наиболее активный представитель топических ингибиторов кальциневрина. Предназначен для лечения АД средней тяжести и тяжелого течения, в том числе стероидрезистентных форм. Многочисленные клинические исследования продемонстрировали, что такролимус обладает эффективностью, сравнимой с таковой сильных ГКС, при этом лишен присущих ГКС побочных эффектов (в частности, не вызывает атрофии кожи) [5]. Показаниями к назначению такролимуса являются среднетяжелое и тяжелое течение АтД в случае резистентности к стандартной терапии. У детей применяется 0,03%-я мазь таролимус. Режим применения — 2 раза в день ежедневно до достижения очищения кожи. Двухкратный режим дозирования должен использоваться не дольше 3 недель, далее мазь наносится однократно. Клинический эффект достигается как правило в течение первой недели. У пациентов, подверженных частым рецидивам заболевания, такролимус необходимо наносить на все обычно поражаемые при обострениях участки кожи 1-2 раза в неделю (перерыв между нанесениями должен составлять 2-3 дня). При возникновении обострения — вновь перейти на режим применения 2 раза в день. Если в течение 6 недель не удается достигнуть улучшения, при переходе на поддерживающий режим дозирования препарата возникает обострение — дальнейшее использование препарата нецелесообразно. Длительность профилактического использования такролимуса — 12 месяцев, затем необходимо провести освидетельствование пациента для принятия решения, продолжать или отменить терапию такролимусом. Во время курса лечения необходимо избегать инсоляции, использовать фотозащитный крем на открытые участки кожи, обрабатываемые мазью такролимус.
Наиболее частые побочные эффекты — покраснение, чувство жжения, усиление зуда на участках обрабатываемых такролимусом. Эти симптомы беспокоят, как правило, в первые дни лечения и разрешаются к концу первой недели. Тяжесть их коррелирует с остротой атопического дерматита. Охлаждение мази в холодильнике перед нанесением и использование увлажняющего средства за 10-15 минут до мази ТИК уменьшает выраженность реакции. Эффекты раздражения кожи можно уменьшить, применяя ацетилсалициловую кислоту внутрь.
Вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази такролимус. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней.
Пимекролимус 1%-й крем показан при атопическом дерматите легкого и среднетяжелого течения и может применяться у детей старше 3 месяцев. Однако в ряде стран Европы, США и Канаде пимекролимус разрешен к применению у детей старше 3 лет. Препарат обладает выраженным действием на большинство штаммов Malazessia, что может быть полезно в случаях сенсибилизации к этому грибу [3]. В 2013 году рядом авторов предложен новый алгоритм терапии атопического дерматита легкой и средней тяжести с применением 1%-го крема пимекролимус [13]. При длительно существующем АтД легкой степени тяжести препарат используется дважды в день при появлении первых признаков обострения. Острый АтД легкой и средней тяжести: на протяжении 3-4 дней использование ТКС, с дальнейшим назначением пимекролимуса дважды в день на все пораженные участки до исчезновения симптомов. Предложено проведение поддерживающей терапии длительностью до 3 месяцев 1 раз в день или реже, по усмотрению лечащего врача, на ранее пораженных участках кожи для предотвращения обострений заболевания.
Активированный пиритион цинка (аэрозоль 0,2%, крем 0,2% и шампунь 1%) является нестероидным препаратом, обладающим широким спектром фармакологических эффектов. Может применяться у детей от 1 года, допускается использование на всех участках тела без ограничений по площади. Препарат снижает колонизацию кожи Malassezia furfur, другими грибами, а также S. aureus, участвующими в патогенезе атопического дерматита. Его применение сопровождается уменьшением выраженности кожного зуда, уменьшением степени тяжести и активности кожного процесса, снижением потребности в использовании топических и антигистаминных препаратов. Крем наносят 2 раза в сутки, возможно применение под окклюзионную повязку. Аэрозоль используют в случаях выраженного мокнутия, распыляют с расстояния 15 см 2-3 раза в сутки [2].
Таким образом, современный интегральный подход к терапии АтД включает ступенчатое использование ТГКС, ТИК или других противовоспалительных средств, постоянное использование базовой терапии эмолиентами, бережное очищение кожи, своевременное назначение наружных антисептиков, антибактериальных, противогрибковых препаратов.
ЛИТЕРАТУРА
1. Российский национальный согласительный документ по атопическому дерматиту. Под ред. Хаитова P.M., Кубановой А.А.. Атопический дерматит: рекомендации для практических врачей. М.: Фармарус принт, 2002, 24 с.
2. Федеральные клинические рекомендации по ведению больных атопическим дерматитом. Российское общество дерматовенерологов и косметологов. М., 2015.
3. Аллергология и иммунология. Клинические рекомендации для педиатров. Под общ. ред. Баранова А.А., Хаитова P.M. М., Союз педиатров России, 2011, 255 с.
4. Феденко Е.С., Филимонова Т.М., Елисютина О.Г., Штырбул О.В., Ниязов Д.Д. Патогенетическое обоснование интегрального подхода к наружной терапии атопического дерматита // Российский аллергологический журнал, 2012; 4: 50-55.
5. Кубанова А.А., Прошутинская Д.В., Текучева Л.В., Авдиенко И.Н. Интегральный подход к наружной терапии атопического дерматита // Вестник дерматологии и венерологии, 2010; 1:20-26.
6. Балаболкин И.И., Гребенюк В.Н., Капустина Е.Ю. Наружное лечение атопического дерматита у детей // Педиатрия, 2007; 86; 2: 93-98.
7. Ревякина В.А. Современные подходы к наружной терапии атопического дерматита у детей // Лечащий врач, 2010, № 1.
8. Leung T.N., Chow С.М., Chow М.Р. et al. Clinical guidelines on management of atopic dermatitis in children. Hong Kong J. Paediatr. (new series), 2013; 18: 96-104.
9. Darsow U., Wollenberg A., Simon D. et al. ETFAD / EADV Eczema Task Force 2009 position paper on diagnosis and treatment of atopic dermatitis // J. Eur. Acad. Dermatol. Venereol, 2010, 24: 317-328.
10. Chiang C., Eichenfield L.F. Quantitative assessment of combination bathing and moisturizing regimens on skin hydration in atopic dermatitis // Pediatr. Dermatol, 2009; 26: 273-278.
11. Атопический дерматит у детей. Пособие для врачей. Под ред.Балаболкина И.И. М., 2006, 55 с.
12. Wollenberg A., Frank R., Kroth J. et al. Proactive therapy of atopic eczema — an evidence-based concept with a behavioral background // J. Dtsch. Dermatol. Ges., 2009; 7: 117-121.
13. Аллергия у детей: от теории к практике. Под ред.й Намазовой-Барановой Л.С. М., 2010-2011,667 с.
14. Lee Y.B., Park H.J., Kwon M.J., Jeong S.K., Cho S.H. Beneficial effects of pseudoceramide-containing physiologic lipid mixture as a vehicle for topical steroids // Eur. J. Dermatol., 2011 Sep-Oct; 21:5:710-6.
15. Luger Т., De Raeve L., Gelmetti C., Kakourou T. et al. Recommendations for pimecrolimus 1% cream in the treatment of mild-to-moderate atopic dermatitis: from medical needs to a new treatment algorithm // Eur. J. Dermatol, 2013 Nov-Dec; 23 (6): 758-66.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник


